Énoncé
Exercice sur 10 points
Le colorant E127, de couleur rouge, est utilisé pour teinter certains aliments comme les cerises confites. Il est également présent dans des médicaments comme les révélateurs de plaque dentaire. C'est un composé ionique, de formule brute Na2C20H6I4O5, noté plus simplement Na2Ery, présent en solution sous la forme d'ions Na+ et Ery2−. Les ions Ery2− constituent l'une des trois formes acide-base de l'érythrosine.
Les objectifs de l'exercice sont d'étudier le dosage de ce colorant dans un révélateur de plaque dentaire, la synthèse de la forme la plus acide, notée H2Ery, de l'érythrosine et la cinétique de la décoloration de celle-ci par l'eau de Javel.
Les objectifs de l'exercice sont d'étudier le dosage de ce colorant dans un révélateur de plaque dentaire, la synthèse de la forme la plus acide, notée H2Ery, de l'érythrosine et la cinétique de la décoloration de celle-ci par l'eau de Javel.
Données
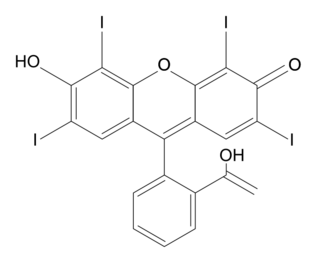
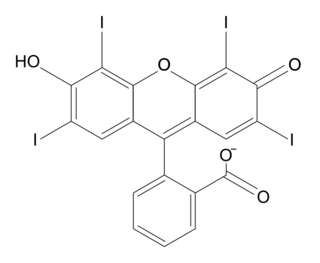
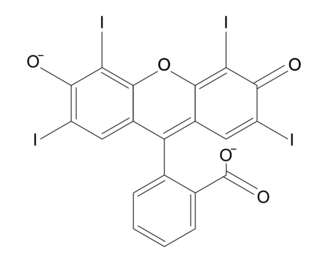
• écriture simplifiée et formule topologique des différentes formes acide-base associées à l'érythrosine :
| Écriture simplifiée | H2Ery | HEry− | Ery2− | |||
| Formule topologique |
|
|
|
• valeurs de pKA à 25 °C des couples acide-base associés à l'érythrosine :
- H2Ery / HEry− : pKA1 = 2,4 ;
- HEry− / Ery2− : pKA2 = 3,8.
• valeurs de masses molaires de quelques espèces :
| Nom | Colorant E127 | Forme la plus acide de l'érythrosine | Forme la plus acide de la fluorescéine | Diiode |
| Écriture simplifiée ou formule brute | Na2Ery | H2Ery | H2Flu | I2 |
| Masse molaire (g · mol−1) | 880 | 836 | 332 | 254 |
Partie 1. Dosage du colorant E127 dans un révélateur de plaque dentaire
Un révélateur de plaque dentaire est une solution vendue en pharmacie permettant d'améliorer le brossage des dents. Elle est préparée à partir du colorant E127.
Données :
• masse volumique du révélateur de plaque dentaire étudié : ρ = 1,0 g mL−1 ;
• pH du révélateur de plaque dentaire étudié : pH = 7,0 ;
• cercle chromatique :
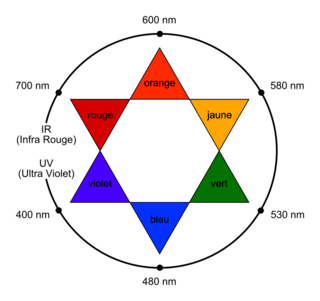 |
• spectre d'absorption d'une solution aqueuse du colorant E127 de concentration en soluté apporté égale à 1,7 × 10−5 mol L−1 et de pH égal à 7,0 :
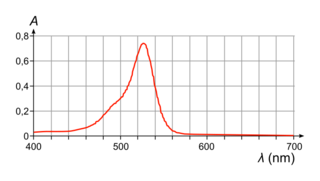 |
1. À l'aide de la formule topologique de la forme H2Ery de l'érythrosine ci-dessous, nommer les familles fonctionnelles associées aux groupes caractéristiques A, B et C.
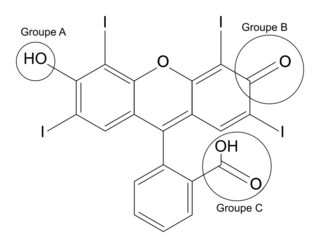 |
Observez la représentation de la molécule. Chaque groupe entouré appartient à une famille fonctionnelle différente. Attention à ne pas les assimiler aux groupes fonctionnels.
2. Identifier, en justifiant, la forme de l'érythrosine qui prédomine dans le révélateur de plaque dentaire étudié.
Le pH du révélateur de plaque dentaire est donné dans l'énoncé. Le diagramme de prédominance des différentes formes d'érythrosine permet d'identifier l'espèce prédominante au pH du révélateur.
Sur le site du fabricant, il est indiqué que le révélateur de plaque dentaire, de couleur rouge, est une solution hydroalcoolique contenant le colorant E127 à 2 % en masse.
Afin de vérifier l'indication précédente sur le titre massique, on réalise les expériences décrites ci-dessous. Préparation de la solution à doser :
Afin de vérifier l'indication précédente sur le titre massique, on réalise les expériences décrites ci-dessous. Préparation de la solution à doser :
- on introduit 0,5 mL de révélateur de plaque dentaire dans une fiole jaugée de 2,0 L que l'on complète avec de l'eau distillée : on obtient la solution S.
- à partir d'une solution aqueuse de colorant E127 de concentration en soluté apporté égale à 1,7 × 10−5 mol L−1, on prépare par dilution six solutions filles ;
- on mesure l'absorbance de chacune de ces solutions à une longueur d'onde appropriée ; les mesures sont reportées sur le graphe de la figure 1 ;
- on mesure l'absorbance de la solution S à la même longueur d'onde ; on obtient A = 0,484.
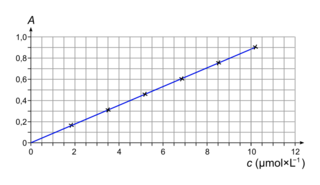 |
3. Justifier la couleur rouge du révélateur de plaque dentaire étudié.
Déterminez le maximum d'absorption avec le spectre d'absorption. La couleur du révélateur correspond à la couleur complémentaire de celle déterminée avec le spectre d'absorption.
4. Après avoir montré que la concentration du colorant E127 apporté dans le révélateur de plaque dentaire est égale à 2,2 × 10−2 mol L−1, déterminer la valeur du titre massique en colorant E127 du révélateur de plaque dentaire analysé. Commenter.
Le candidat est invité à prendre des initiatives et à présenter la démarche suivie, même si elle n'a pas abouti. La démarche est évaluée et nécessite d'être correctement présentée.
Le candidat est invité à prendre des initiatives et à présenter la démarche suivie, même si elle n'a pas abouti. La démarche est évaluée et nécessite d'être correctement présentée.
La courbe d'étalonnage et la mesure de l'absorbance de la solution permettent de déterminer la concentration de la solution S. Or, la solution S a été diluée donc la concentration de la solution mère puis celle du titre massique de la solution mère permettent de conclure.
Partie 2. Synthèse de l'érythrosine à partir de la fluorescéine
L'érythrosine peut être synthétisée à partir d'un autre colorant, la fluorescéine, en présence d'acide iodique et d'éthanol ; l'équation de la réaction modélisant cette synthèse est donnée ci-dessous :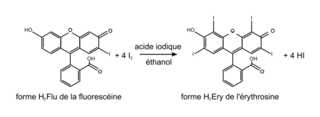 |
Dans une publication scientifique, on trouve les informations suivantes :
• les différentes étapes d'un protocole de synthèse de l'érythrosine :
– étape n° 1 :
réaliser la synthèse de la forme H2Ery de l'érythrosine à partir de 5,0 g de fluorescéine H2Flu et de 9,5 g de diiode I2, en présence d'éthanol et d'acide iodique ;
chauffer et agiter le mélange pendant deux heures à une température de 60 °C,
– étape n° 2 :
après refroidissement, filtrer le mélange à l'aide d'un filtre Büchner puis laver le solide rouge obtenu avec de l'eau et de l'éthanol,
– étape n° 3 :
mesurer la température de fusion du solide rouge obtenu ;
– étape n° 1 :
réaliser la synthèse de la forme H2Ery de l'érythrosine à partir de 5,0 g de fluorescéine H2Flu et de 9,5 g de diiode I2, en présence d'éthanol et d'acide iodique ;
chauffer et agiter le mélange pendant deux heures à une température de 60 °C,
– étape n° 2 :
après refroidissement, filtrer le mélange à l'aide d'un filtre Büchner puis laver le solide rouge obtenu avec de l'eau et de l'éthanol,
– étape n° 3 :
mesurer la température de fusion du solide rouge obtenu ;
• la valeur du rendement r de la synthèse : r = 59 %.
D'après N. Pietrancosta et al., Bioorganic & Medicinal Chemistry, 18 (2010), 6922, 6933.
5. Identifier le rôle des étapes n° 1, n° 2 et n° 3 du protocole expérimental de synthèse de l'érythrosine.
Chaque étape correspond à un type de réaction chimique ou à une étape expérimentale.
6. Identifier l'opération du protocole expérimental réalisée pour optimiser la vitesse de formation de l'érythrosine.
Déterminez un facteur cinétique qui permette d'accélérer la réaction chimique.
7. Déterminer le réactif limitant de la synthèse de l'érythrosine.
Comparez les quantités de matières initiales des réactifs. Attention à tenir compte de la stœchiométrie de la réaction !
8. Montrer que la masse d'érythrosine de forme H2Ery obtenue expérimentalement est d'environ 4,6 g.
La quantité de matière maximale d'érythrosine obtenue et la valeur du rendement de la réaction permettront de déterminer la quantité de matière expérimentale.
9. Déterminer le nombre de flacons de 10 mL de révélateur de plaque dentaire, de pH égal à 7 et de concentration égale à 2,2 × 10−2 mol L−1 en colorant E127, qu'il est possible de fabriquer grâce à cette synthèse.
La masse précédente donne la quantité de matière d'érythrosine réellement obtenue. Or, on peut calculer la quantité de matière nécessaire par flacon donc le rapport des deux valeurs donnera le nombre de flacons.
Partie 3. Suivi cinétique de la décoloration d'une solution de colorant E127 par l'eau de Javel
Le filtre Büchner utilisé lors de la synthèse précédente est coloré par les résidus de colorant E127 rouge. Pour le décolorer, on peut utiliser de l'eau de Javel.En effet, la forme Ery2− de l'érythrosine réagit avec les ions hypochlorite ClO− contenus dans l'eau de Javel pour former un produit incolore. Cette réaction est supposée totale.
 |
On réalise, à 25 °C, les deux expériences A et B décrites ci-après :
– dans des béchers de 50 mL, deux solutions sont préparées à partir d'une solution commerciale d'eau de Javel de concentration en ions hypochlorite égale à 0,73 mol L−1 :
| Solution | SA | SB |
|---|---|---|
| Volume d'eau de Javel (mL) | 5 | 10 |
| Volume d'eau distillée (mL) | 5 | 0 |
– pour l'expérience A :
• à la date t = 0 s, on verse dans le bécher contenant la solution SA un volume de 10,0 mL d'une solution aqueuse de colorant E127 de concentration en soluté apporté égale à 1,7 × 10−5 mol L−1,
• on remplit rapidement une cuve spectrophotométrique avec le mélange réactionnel, on l'introduit dans un spectrophotomètre réglé à une longueur d'onde appropriée et on relève les valeurs d'absorbance en fonction du temps ;
– pour l'expérience B, on recommence les mêmes opérations avec la solution SB.
Dans chacun des mélanges réactionnels préparés, l'érythrosine est présente sous la seule forme Ery2− et cette forme est la seule espèce qui absorbe à la longueur d'onde choisie.
Les résultats obtenus permettent de tracer la courbe d'évolution de la concentration en quantité de matière de la forme Ery2− de l'érythrosine pour l'expérience A et B (figure 2).
Les résultats obtenus permettent de tracer la courbe d'évolution de la concentration en quantité de matière de la forme Ery2− de l'érythrosine pour l'expérience A et B (figure 2).
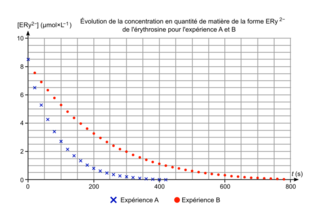 |
10. Décrire qualitativement, en exploitant la figure 2, l'évolution de la vitesse volumique de disparition de la forme Ery2− de l'érythrosine au cours du temps pour l'expérience A. Proposer un facteur cinétique à l'origine de cette évolution.
La vitesse volumique de disparition de l'érythrosine en un point correspond à la pente de la tangente à la courbe au point considéré.
11. Déterminer graphiquement le temps de demi-réaction pour l'expérience A. Commenter.
Le temps de demi-réaction correspond à l'abscisse du point correspondant à la moitié de la concentration initiale en érythrosine.
12. Expliquer comment il est possible d'optimiser la décoloration du filtre Büchner.
Analysez les deux courbes données afin de déterminer un autre facteur cinétique.
Corrigé
Partie 1. Dosage du colorant E127 dans un révélateur de plaque dentaire
1.
 |
Le groupe A appartient à la famille des alcools.
Le groupe B appartient à la famille des cétones.
Le groupe C appartient à la famille des acides carboxyliques.
Le groupe B appartient à la famille des cétones.
Le groupe C appartient à la famille des acides carboxyliques.
2. D'après l'énoncé, le pH du révélateur de plaque dentaire étudié est de 7,0. Traçons le diagramme de prédominance :
 |
Pour pH = 7,0 on est dans le domaine de prédominance de Ery2−.
3. Le spectre d'absorption du colorant E127 montre un maximum d'absorption pour λ = 525 nm environ. Le cercle chromatique montre que cette absorption correspond à la couleur complémentaire (donc de la solution) rouge. La solution est donc rouge.
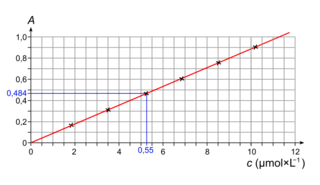
4. On trace la droite passant par tous les points.
 |
Partie 2. Synthèse de l'érythrosine à partir de la fluorescéine
L'absorption de la solution S est A = 0,484, ce qui correspond, avec la courbe d'étalonnage précédente, à cS = 5,5 µmol/L.
Or, S correspond à 0,5 mL de révélateur complété à 2,0 L avec de l'eau distillée.
Soit n = c × V = 5,5 × 10−6 × 2,0 = 1,1 ×10−5 mol
Ce qui donne une concentration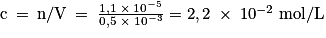
Le titre massique en colorant E127 est le pourcentage en masse du colorant soit :
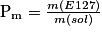
or m(E127) = n × M = 2,2 × 10−2 × 880 = 19 g
et m(sol) = ρ × V = 1,0 × 10−3 g
Soit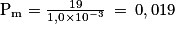 = 1,9 %.
= 1,9 %.
Le résultat trouvé est en concordance avec les données du fabricant.
Or, S correspond à 0,5 mL de révélateur complété à 2,0 L avec de l'eau distillée.
Soit n = c × V = 5,5 × 10−6 × 2,0 = 1,1 ×10−5 mol
Ce qui donne une concentration
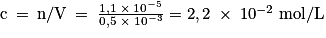
Le titre massique en colorant E127 est le pourcentage en masse du colorant soit :
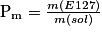
or m(E127) = n × M = 2,2 × 10−2 × 880 = 19 g
et m(sol) = ρ × V = 1,0 × 10−3 g
Soit
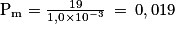 = 1,9 %.
= 1,9 %.Le résultat trouvé est en concordance avec les données du fabricant.
5. L'étape n° 1 est une transformation chimique, c'est une réaction de substitution.
L'étape n° 2 est la cristallisation et l'extraction de l'érythrosine.
L'étape n° 3 est l'identification du produit obtenu par mesure de la température.
L'étape n° 2 est la cristallisation et l'extraction de l'érythrosine.
L'étape n° 3 est l'identification du produit obtenu par mesure de la température.
6. On chauffe le mélange réactionnel. Or, la température est un facteur cinétique donc le chauffage permet d'accélérer la synthèse : elle augmente la vitesse de formation de l'érythrosine.
7. Calcul de la quantité de matière :
On a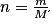
On a
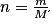
• pour le I2, on trouve 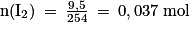 ;
;
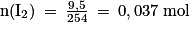 ;
;• pour le H2Flu, on trouve 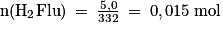 .
.
Or, pour être dans les proportions stœchiométriques, il faudrait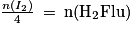
Ici on note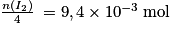 donc
donc 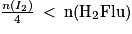
Le diiode I2 est le réactif limitant.
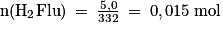 .
.Or, pour être dans les proportions stœchiométriques, il faudrait
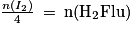
Ici on note
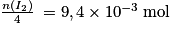 donc
donc 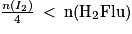
Le diiode I2 est le réactif limitant.
8. La quantité maximale est donnée par la quantité de réactif limitant n(H2Ery) = 9,4 ×10−3 mol
Donc la masse maximale est mmax (H2Ery) = n × M = 9,4 × 10−3 × 836 = 7,8 g
Or le rendement est r = 59 %
La masse expérimentale obtenue est mexp (H2Ery) = 7,8 × 0,59 = 4,6 g
Donc la masse maximale est mmax (H2Ery) = n × M = 9,4 × 10−3 × 836 = 7,8 g
Or le rendement est r = 59 %
La masse expérimentale obtenue est mexp (H2Ery) = 7,8 × 0,59 = 4,6 g
9. La quantité expérimentale de H2Ery formée est 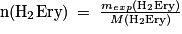
Et on a synthétisé 4,6 g d'érythrosine.
On a donc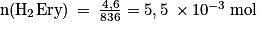
Or, chaque flacon doit contenir une solution de concentration égale à 0,022 mol/L.
Soit une quantité égale à n = C × V = 0,022 × 10 × 10−3 = 2,2 × 10−4 mol dans chaque flacon
On aura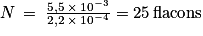 .
.
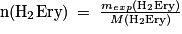
Et on a synthétisé 4,6 g d'érythrosine.
On a donc
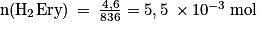
Or, chaque flacon doit contenir une solution de concentration égale à 0,022 mol/L.
Soit une quantité égale à n = C × V = 0,022 × 10 × 10−3 = 2,2 × 10−4 mol dans chaque flacon
On aura
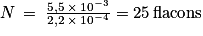 .
.Partie 3. Suivi cinétique de la décoloration d'une solution de colorant E127 par l'eau de Javel
10. La vitesse volumique de disparition de Ery2− correspond au coefficient directeur de la tangente à la courbe donnée.
Comme Ery2− est consommé, alors le coefficient directeur est négatif.
Au début, la vitesse est grande.
Au cours du temps, la vitesse diminue.
Le facteur cinétique à l'origine de cette évolution est la concentration en Ery2− qui est un réactif et qui diminue progressivement.
Comme Ery2− est consommé, alors le coefficient directeur est négatif.
Au début, la vitesse est grande.
Au cours du temps, la vitesse diminue.
Le facteur cinétique à l'origine de cette évolution est la concentration en Ery2− qui est un réactif et qui diminue progressivement.
11. Le temps de demi-réaction est la durée nécessaire pour que la concentration de ce réactif ait diminué de moitié.
On a la concentration à t = 0 s de [Ery2−] = 8,5 µmol/L.
On cherche l'abscisse du point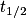 pour une concentration [Ery2−] = 4,3 µmol/L.
pour une concentration [Ery2−] = 4,3 µmol/L.
On lit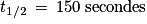 .
.
La réaction de décoloration est terminée au bout de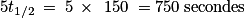 soit plus de 12 minutes, ce qui est long.
soit plus de 12 minutes, ce qui est long.
On a la concentration à t = 0 s de [Ery2−] = 8,5 µmol/L.
On cherche l'abscisse du point
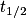 pour une concentration [Ery2−] = 4,3 µmol/L.
pour une concentration [Ery2−] = 4,3 µmol/L.On lit
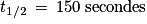 .
.La réaction de décoloration est terminée au bout de
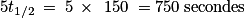 soit plus de 12 minutes, ce qui est long.
soit plus de 12 minutes, ce qui est long.12. On souhaite que la décoloration soit plus rapide et donc que Ery2− disparaisse plus rapidement.
La figure 2 montre que le temps de demi-réaction est plus faible dans le cas de l'expérience B.
Or, on constate que, dans l'expérience B, on a utilisé de l'eau de Javel sans la diluer, contrairement à l'expérience A.
Il faut donc utiliser de l'eau de Javel plus concentrée pour ainsi avoir un temps de demi-réaction de 50 secondes au lieu de 150 secondes.
La figure 2 montre que le temps de demi-réaction est plus faible dans le cas de l'expérience B.
Or, on constate que, dans l'expérience B, on a utilisé de l'eau de Javel sans la diluer, contrairement à l'expérience A.
Il faut donc utiliser de l'eau de Javel plus concentrée pour ainsi avoir un temps de demi-réaction de 50 secondes au lieu de 150 secondes.